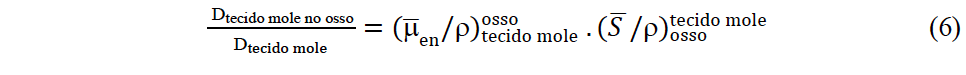INOMOGENEIDADE DE TECIDOS ÓSSEOS
André Lima de Souza Castro*; Tarcísio Passos Ribeiro Campos**
*Físico Médico do Instituto de Radioterapia São Francisco e do Centro de Tratamento
em Radioterapia. Departamento de Engenharia Nuclear – UFMG.
**Professor, Doutor do Departamento de Engenharia Nuclear – UFMG.
maio de 2017
Introdução
A radioterapia é uma modalidade clinica que utiliza radiações ionizantes para o tratamento curativo, profilático ou paliativo de doenças malignas ou benignas. Quando essas lesões estão localizadas em profundidade emprega-se, preferencialmente, a irradiação com feixes de fótons capazes de penetrar e transferir energia ao meio através dos mecanismos de interação (HALPERIN et al., 2007). Além das características intrínsecas do feixe de radiação, como por exemplo seu espectro de energia, o processo de interação dos fótons com o meio é influenciado pelas diferentes propriedades materiais constituintes do ser humano. Inomogeneidades de tecido como pulmão, cavidades de ar, ossos ou implantes metálicos, perturbam o transporte dos fótons primários e de elétrons secundários produzidos nas interações, consequentemente, alteram a distribuição espacial da dose (LEVITT et al, 2006). É essencial o conhecimento de como a dose absorvida é afetada pela presença dessas inomogeneidades a fim de maximizar o benefício terapêutico e estimar a probabilidade de complicação dos tecidos normais.
Encontra-se na literatura diversos trabalhos abordando a perturbação da dose absorvida no interior ou na interface de tecidos de baixo número atômico (Z) como pulmão e cavidades de ar (WHITE et al, 1996; KAN et al, 1998; WANG et al, 2001; FRANKS et al, 2010, NAKAYAMA et al, 2014; ZARZA-MORENO et al, 2014; NOGUEIRA et al, 2015). Um número expressivo de trabalhos investiga, também, a influência de tecidos de alto Z sobre dose absorvida (DAS, KHAN,1989; LI et al., 1999; NADROWITZ, FEYERABEND, 2001; AAPM TG63, 2003; MIAN et al.,1987; STEFAN et al.,2009; De CONTO et al, 2014). No entanto, dentro dessa classe, há um número restrito de autores investigando efeitos de inomogeneidade de tecidos ósseos. Nesse contexto o presente trabalho objetiva abordar os conceitos fundamentais da interação da radiação com esses tecidos e sua importância para a radioterapia.
Fundamentação teórica
Interação da radiação eletromagnética com o tecido
Na interação de fótons com a matéria a atenuação e a transferência de energia para o meio é dominada por processos de grande importância na radioterapia. Nesse trabalho foram destacados apenas três processos considerados mais relevantes para a compreensão da interação com tecidos ósseos.
Efeito fotoelétrico
O efeito fotoelétrico é um fenômeno no qual um fóton de energia hν interage com um átomo que absorve essa energia e a transfere para um elétron de sua nuvem eletrônica que é ejetado (EISBERG, RESNICK, 1994). Há possibilidade desse elétron ejetado causar outras ionizações e, portanto, transferir energia ao meio. A energia cinética do fotoelétron Ec é igual a diferença entre a energia do fóton incidente hν a energia de ligação Elig desse elétron na nuvem eletrônica, tal que:
A vacância gerada pelo elétron ejetado pode ser ocupada por um elétron livre capturado do meio ou pelo rearranjo dos elétrons de camadas mais energéticas com subsequente emissão de raios X característicos. Há, também, a possibilidade de emissão de elétrons Auger, monoenergéticos, produzidos pela absorção interna daqueles raios X característicos. Esses eventos também tem probabilidade de provocar outras ionizações no meio (EISBERG, RESNICK, 1994). O efeito fotoelétrico é o modo de interação predominante para fótons considerados de baixa energia, da ordem de grandeza de keV. A probabilidade dessa interação também aumenta para tecidos constituintes de elementos com maiores números atômicos. De acordo com KNOLL, 2000, não existe uma expressão analítica única válida para representar a probabilidade da absorção fotoelétrica (τ) por átomo para todas as energias e números atômicos e, uma expressão geral sugerida é dada por:
em que C é uma constante, Z o número atômico do meio e E a energia do fóton incidente. Os coeficientes n e m possuem valores diversos dependendo do material e energia do fóton (KNOLL, 2000).
Espalhamento Compton
Neste processo, o fóton interage com um elétron considerado livre, ou seja, a energia de ligação desse elétron é muito menor que a energia do fóton incidente. Na interação, o fóton é defletido em determinado ângulo em respeito à direção inicial e a energia é transferida para o elétron que também é espalhado. Devido à possibilidade de deflexão em todos os ângulos, a energia transferida ao elétron pode variar de zero a uma fração considerável da energia do fóton. Esse elétron tem probabilidade de transferir energia ao meio através de processos de ionização e o fóton espalhado pode interagir novamente com o meio e causar ionizações secundárias (KNOLL, 2000; EISBERG, RESNICK, 1994).
Uma vez que a interação Compton envolve elétrons essencialmente livres no tecido absorvedor, ela independe do número atômico. O coeficiente de atenuação por massa do Efeito Compton depende apenas da densidade mássica de elétrons, isto é número de elétrons por grama. Embora essa quantidade descrita decresça suave mas sistematicamente com o número atômico dos elementos, exceto o hidrogênio, a maioria dos tecidos contem semelhante número de elétrons por unidade de massa (KHAN, 2003), como reportado na Tabela1. Portanto, se a energia de um feixe de fótons situa-se na região onde o Efeito Compton predomina, ou seja, da ordem de MeV, a absorção da energia pelos tecidos ocorrerá de maneira semelhante, diferindo pouco apenas devido à densidade mássica dos tecidos. Efeitos mais importantes ocorrem em regiões de interface entre tecidos com elevadas diferenças nas densidades mássica e eletrônicas, em que uma região de desequilíbrio eletrônico existe e a absorção da energia devido aos elétrons espalhados na primeira interação e elétrons secundários é alterada (AAPM TG 85, 2004).
Produção de pares
O fóton de alta energia interage com o campo eletromagnético do núcleo atômico e tem sua energia completamente absorvida na criação de um par elétron-pósitron. Uma vez que há a conversão de energia do fóton em massa, existe um limiar de energia, igual a duas vezes a energia de repouso do elétron (1,02 MeV), necessária para a produção de pares ocorrer. Energias de fótons superiores a esse limiar podem ser transformadas em energias cinéticas de elétrons e pósitrons criados. Esses elétrons podem interagir com o meio causando ionizações secundárias induzidos pela interação do fóton. Já os pósitrons serão aniquilados, subsequentemente, pelo meio absorvedor e dois fótons antiparalelos são produzidos. Esses fótons, consequentemente, tem probabilidade de interagir com o meio e causar ionizações que resultarão em transferência de energia à matéria (KNOLL, 2000; KHAN, 2003)
A probabilidade de ocorrência da produção de pares varia, aproximadamente, com o quadrado do número atômico do meio. Além disso, para um dado material, a chance de interação aumenta com o logaritmo da energia do fóton incidente, acima do limiar (PODGORSAK, 2005).
Interação de partículas carregadas com o tecido
As interações de fótons descritas transferem energia para partículas carregadas incluindo principalmente fotoelétrons, elétrons Compton e pares elétron-pósitron, que interagem com a matéria predominantemente, por ionização ou excitação (AAPM TG 85, 2004; KHAN, 2003). À medida que um elétron energético percorre a matéria, interações coulombianas com elétrons orbitais e núcleos atômicos ocorrem. Então, de forma inelástica e elástica, o elétron interage e transfere sua energia cinética para o meio, alterando sua trajetória. As perdas energéticas colisionais ou radioativas são descritas pelo stopping power (KNOLL, 2000). As inúmeras colisões na interação de elétrons com o meio são descritas por uma teoria estatística de múltiplos espalhamentos. No espalhamento elástico o elétron é defletido do percurso original mas nenhuma energia é transferida para o meio. Na colisão inelástica o elétron sofre espalhamento e transfere parte de sua energia para um elétron orbital ou a converte como radiação Bremsstrahlung (AAPM TG 85, 2004). A perda inelástica de energia média do elétron se movendo em uma distância dl em um meio de densidade r é dada pelo stopping power total em unidades J.m2.kg-1, definida como segue:
O stopping power total (S/ρ)tot consiste de duas componentes: o stopping power de colisão, resultante de interações de ionização e excitação com elétrons orbitais; e, o stopping power de radiação, resultante, predominantemente, da interação com o núcleo atômico.Considerando apenas a deposição local de energia, o stopping power de colisãoé a grandeza mais relevante para o processo (PODGORSAK, 2005).
Essa grandeza depende da energia e do número atômico do meio e pode ser considerado aproximadamente independente da densidade. Elétrons perdem variadas quantidades de energia em cada interação e por simplicidade assume-se aproximadamente uma redução contínua da energia cinética, do inglês continuous slowing down approximation (CSDA). Isso permite a determinação de um alcance das partículas secundárias associadas a um CSDA, RCSDA, único, em unidade kg.m-1.
Uma vez que partículas carregadas produzidas por feixes de fótons de baixa energia possuem alcance curto, é possível aceitar um tratamento simplificado para a interação desses elétrons. Para energias de fótons mais altas os alcances dos elétrons são significativamente mais longos e a distribuição da energia dessas partículas carregadas produzidas pelo feixe de fótons deve ser modelada (AAPM TG 85, 2004). Esses elétrons podem ter energia suficiente para causar outras ionizações e excitações e produzir elétrons secundários que ao interagirem com o meio também contribuem para o aumento da dose absorvida. A Tabela 2 exibe o alcance de elétrons secundários RCSDA em diferentes tecidos e para distintas energias incidentes de fótons.
Os múltiplos espalhamentos sofridos pelos elétrons redirecionam suas energias e alteram o padrão de deposição de dose. Quando o elétron é espalhado em ângulos elevados, o fenômeno de backscattering, ou retroespalhamento, pode ocorrer. Os elétrons de backscattering não trasnfe-rem toda sua energia no meio absorvedor e são responsáveis por alterar a distribuição da dose absorvida em regiões de inomogeneidade, espe-cialmente, nas interfaces de tecidos com baixo número atômico e alto número atômico (KNOLL,2000; KHAN,2003). De forma aproximada a pro-babilidade de espalhamento varia com o quadrado do número atômico do meio absorvedor e inversamente com o quadrado da energia cinética do elétron (PODGORSAK, 2005). No entanto, devido à natureza aleatória desses eventos o cálculo detalhado dos múltiplos espalhamentos dos elétrons e de suas deposições de dose requerem métodos estocásticos de Monte Carlo.
Inomogeneidade de tecidos ósseos
Inomogeneidades de dose introduzidas pela presença de tecidos ósseos podem resultar principalmente em mudanças na absorção do fóton pri-mário e no padrão de espalhamento de fótons ou em perturbações locais da fluência de elétrons secundários conhecidas como efeitos de inter-face. A importância relativa desses efeitos depende do número atômico, densidade e dimensão da inomogeneidade, qualidade da radiação, geo-metria e tamanhos de campos (DAS, 1989; AAPM TG 63, 2003).
Com o intuito de quantificar matematicamente o efeito da atenuação causado pelo osso pode-se calcular a absorção de dose relativa entre teci-dos em distancias superiores ao alcance de elétrons secundários, em condições de equilíbrio eletrônico para uma dada fluência de energia de fótons, através da razão dos coeficientes de absorção de energia em massa chamado também de fator f (KHAN, 2003).
Após a inomogeneidade, a dose é atenuada devido à maior densidade eletrônica do osso em relação ao tecido mole vizinho a magnitude da atenuação depende também da qualidade da radiação. Para radiações com energias da ordem kV, em que o efeito fotoelétrico é predominante, tecidos com maior número atômico, como é o caso do osso, tem uma maior secção de choque para o efeito fotoelétrico e sua probabilidade de absorção da radiação será maior. Como resultado há um aumento da dose nas primeiras camadas de osso seguida por uma redução devido à atenuação nos tecidos situados além da inomogeneidade. Para energias da ordem de megavoltagem, a dose absorvida pelo osso é sutilmente menor que para o tecido mole vizinho devido à diminuição da secção de choque para o efeito fotoelétrico, logo o efeito de atenuação se torna menos importante, embora ainda existente (JOHNS, CUNNINGHAM, 1983).
Efeitos de interface são também experimentados em tecidos moles presentes no interior dos ossos como vasos sanguíneos, canal Haversiano, osteócitos e medula. Quando a espessura do tecido mole no osso é menor que o alcance dos elétrons, as interações dos fótons nessa cavidade podem ser ignoradas e, a ionização é considerada inteiramente por elétrons Comptons, fotoelétrons ou elétrons de produção de pares originados no material circundante (ATTIX, 1986; KHAN, 2003).
A razão da dose de um tecido mole no osso em relação à dose em um meio homogêneo assumindo uma fluência de fótons constante é:
Em que [μen/ρ](tecido mole-osso) foi definido anteriormente, e [𝑆 /ρ](osso-tecido mole) é a razão dos stopping powers médios de colisão em massa do tecido mole em relação ao osso para elétrons.
Valores calculados dessa razão são exibidos na Tabela 3. Os dados mostram que para a mesma fluência de fótons, tecidos moles inseridos em ossos absorverão maiores doses em comparação com o osso ou tecidos mole na ausência do osso. Isso ocorre porque (μen/ρ) é maior para o osso que para o tecido mole na região de baixas energias de fótons devido a maior probabilidade de efeito fotoelétrico e na região de altas energias devido à maior probabilidade de produção de pares. Entretanto, para a faixa de energia em que o efeito Compton predomina, [μen/ρ] é sensivelmente menor. Por sua vez, [𝑆/ρ] é maior para o tecido mole em todas as faixas de energia porque contém maior número de elétrons por unidade de massa que o osso, ver Tabela 1. Consequentemente, o efeito combinado é responsável por aumentar a dose absorvida no tecido mole inserido no osso em relação ao meio circundante (KHAN, 2003).
Discussão
Uma breve revisão da literatura referente a experimentos investigando efeitos de interface de tecidos ósseos mostra que a metodologia empregada na maioria dos trabalhos baseia-se, principalmente, em medidas com dosímetros termoluminescentes (TLD) ou filmes radiológicos para mensurar a absorção, atenuação da dose e efeitos de interface osso/tecido mole e comparações com os valores preditos pelas ferramentas de cálculo existentes. Spiers em 1951 discutiu o problema da dose absorvida em tecidos moles inclusos pelos canais Harversianos do osso irradiado com raios X e gama. Concluiu que a dose é dependente do tamanho da cavidade, comprimento de onda da radiação e que os cálculos empregados na época estavam de acordo com as observações experimentais relevantes disponíveis. Já em 1962, Sinclair avaliou a dose absorvida na interface osso-tecido a partir de um modelo físico da cavidade da medula de um rato para raios X e gama de diferentes energias e obteve um aumento da dose na interface osso-medula de até 7% para feixes de baixa energia e 1% para energias de fótons emitidos pelo cobalto-60. Investigando a perturbação de dose na interface de tecidos ósseos de alto número atômico com câmaras de ionização de placas paralelas, TLDs e filmes radiológicos, Das (1988) observou que na direção do feixe ocorreu aumento da dose na interface osso-tecido para energias superiores a 10 MV e que esse efeito de interface persistiu por uma distância equivalente ao alcance dos elétrons retroespalhados. Mais recentemente, Saxena e Higgins (2010) avaliaram a heterogeneidade de dose com filmes radiológicos em objetos simuladores de osso para diferentes sistemas de planejamento e seus respectivos métodos de correção de heterogeneidade. Utilizando campos paralelos e opostos os resultados medidos na interface tecido-osso concordaram entre 5% e 10% para os algoritmos de cálculos. Na interface distal do osso, a dose medida foi subestimada de 5% a 10% para os campos testados. Fairbanks et al. (2011) compararam diversos algoritmos de correção de heterogeneidade de um mesmo TPS (do inglês Treatment Planning System) para diferentes tipos de inomogeneidade de tecidos destacando um phantom simplificado de agua sólida e material tecido equivalente ao osso. A dose absorvida foi medida por uma câmara de ionização posicionada posterior à inomogeneidade e comparada com o resultado previsto pelo TPS. A maior discrepância obtida entre todos os algoritmos de correção foi de 5%. Thompson em 2013 em seu trabalho de validação de phantom de cabeça e pescoço e irradiação de glioblastoma multiforme também encontrou um valor de dose absorvida em uma região distal à interface osso-tecido concordando em 5% entre a dose medida por filme radiocrômico e o calculado pelo TPS para uma configuração de três campos.
Uma observação referente é que as medidas realizadas com filme ou com simulação por Monte Carlo diferiram em várias magnitudes dos dados previstos pelos diversos TPSs ou sistemas de cálculo abordados. Observa-se que os resultados encontrados para os trabalhos mais recentes apontam uma menor discrepância entre os valores previstos pelos TPSs e os obtidos por medidas dosimétricas ou simulações por MC devido à evolução matemática dos algoritmos de cálculo utilizados nos TPSs atuais. Adicionalmente, o grau de divergência entre os resultados dos artigos citados pode ser atribuído também à metodologia experimental, já que a influência provocada pelas interfaces de tecido é dependente da extensão da heterogeneidade, composição, localização, energia do feixe, tamanho e geometria de campos (Photon Treatment Planning Collaborative Working group, 1991).
Conclusão
Na prática da radioterapia usualmente o feixe de radiação atravessa tecidos com grande heterogeneidade de composição e formatos, em particular, estruturas anatômicas ósseas. Existem situações clínicas em que a perturbação da dose causadas por essa inomogeneidade pode ser importante. Quando o alvo do tratamento está localizado próximo à um órgão critico, como frequentemente ocorre no tratamento de tumores do sistema nervoso central, a dose é distribuída heterogeneamente devido à alterações na atenuação e fluência dos elétrons secundários causados pela presença de ossos no campo de irradiação. Imprecisões de cálculo têm potencial de afetar o controle tumoral ou aumentar a probabilidade de complicação de tecido normal. Justifica-se, portanto, a necessidade de estudar com metodologias consistentes as intercomparações dosimétricas em regiões de interface de tecido com diferentes propriedades físicas e radiológicas visto que há inúmeras situações, ainda pouco exploradas, relacionadas, à inomogeneidade da dose causada pelo osso.
Referências Bibliográficas
AAPM. AMERICAN ASSOCIATION OF PHYSICS IN MEDICINE. Dosimetric considerations for patients with HIP prostheses undergoing pelvic irradiation. Report of the AAPM Radiation Therapy Committee Task Group 63. Med. Phys. v. 30, n.6, p. 1163-1182. 2003.
AAPM. AMERICAN ASSOCIATION OF PHYSICS IN MEDICINE. Tissue inhomogeneity corrections for megavoltage photon beams. Report of the AAPM Radiation Therapy Committee Task Group 85. 2004. p. 142
ATTIX, F.H. Introduction to Radiological Physics and Radiation Dosimetry. John Wiley & Sons, Inc. ed. 1, 1986. 633p.
DAS, I. J.; KKAN, F. M. Backscatter dose perturbation at high atomic number interfaces in megavoltage photon beams. Med. Phys. v.16, p.367–375. 1989.
De CONTO, C.; GSCHWINDA, R.; MARTINB, E.; MAKOVICKAA, L. Study of dental prostheses influence in radiation therapy. Physica Medica, v.30, n.1, p.117–121. 2014.
EISBERG, R.; RESNICK, R. Física Quântica. Campus, ed. 9. 1994. 928p.
FRANKS, K. N.; PURDIE, T. G.; DAWSON, L. A.; BEZJAK, A.; JAFFRAY, D. A.; BISSONNETTE. J-P. Incorporating Heterogeneity corrections and 4DCT in lung stereotactic body radiation therapy (SBRT): The effect on target coverage, organ-at-risk doses, and dose conformity. Medical Dosimetry, v. 35, n. 2, p. 101-107. 2010.
HALPERIN, E. C.; PEREZ, C. A.; BRADY, L. W. Perez and Brady’s Principles and Practice os Radiation Oncology. Lippincott Williams & Wilkins. 5 ed. 2007. 2050p.
JOHNS, H.E., CUNNINGHAM, J.R. The Physics of Radiology. Charles C Thomas Pub Ltd. ed.4. 1983. 816p.
KAN, W. K.; WU, P. M.; LEUNG, H. T.; LO, T. C.; CHUNG, C. W.; KWONG, D. L. W.; SHAM, S.T. The effect of the nasopharyngeal air cavity on x-ray interface doses. Phys. Med. Biol, v.43, p.529-537. 1998.
KHAN, F. M. The Physics of Radiation Therapy. L pp W a & W k , . 3 Ph a ph a. 2003. 560p.
KNOLL, G. F. Radiation detection and measurement. John Wiley & Sons, Inc. ed. 3. 2000. 816p.
LEVITT, S.H.; PURDY, J.A.; PEREZ, C.A; POORTMAN,P. Technical Basis of Radiation Therapy:Practical Clinical Applications. Springer .4 ed. Berlim. 2006. 856 p.
LI, X. A.; CHU, J. C.; CHENh, W.; ZUSAG, T. Dose enhancement by a thin foil of high-Z material: a Monte Carlo study. Med. Phys. v.26, p.1245–1251. 1999
MIAN, T.A.; VAN PUTTEN Jr. M.C.; KRAMER, D.C.; JACOB, R.F.; BOYER, A.L. Backscatter radiation at bone-titanium interface from high-energy x and gamma rays. International Journal of Radiation Oncology Biology Physics, v13, n. 12, p.1943-1947. 1987.
NADROWITZ, R.; FEYERABEND, T. Backscatter dose from metallic materials due to obliquely incident high-energy photon beams. Med. Phys. v.28, n.6, p.959–965. 2001.
NAKAYAMA, M.; YOSHIDA, K.; NISCHIMURA, H.; MIYAWAKI, D.; UEHARA, K.; OKAMOTO, Y.; OKAYAMA, T.; SASAKI, R. Effect of heterogeneity correction on dosimetric parameters of radiotherapy planning for thoracic esophageal câncer. Medical Dosimety, v.39, p.31-33. 2014.
NIST. NATIONAL INSTITUTE OF STANDARDS AND TECHNOLOGY (A). X-Ray mass attenuation coefficients. Disponível em: <</http://physics.nist.gov/PhysRefData/XrayMassCoef/tab4.html)> Acesso: 13 de Jun de 2014.
NIST. NATIONAL INSTITUTE OF STANDARDS AND TECHNOLOGY (B). Stopping powers and range tables for electrons. Disponível em: <</http://physics.nist.gov/PhysRefData/Star/Text/ESTAR.html)> Acesso: 13 de Jun de 2014.
NOGUEIRA, L. B.; SILVA, H. L. L.; CAMPOS, T. P. R. Experimental dosimetry in conformal breast teletherapy compared with the planning system. Applied Radiation and Isotopes , v. 97, p. 93-100. 2015.
PHOTON TREATMENT PLANNING COLLABORATIVE WORKING GROUP. Role of inhomogeneity corrections in three-dimensional photon treatment planning. Int J Radiat Oncol Biol Phys. v.15, n.21(1), p.59-69. 1991.
PODGORSAK, E. B. Radiation Oncology Physics: A Handbook for Teachers and Students. International Atomic Energy Agency, 2005. 696 p.
STEFAN, I.; KOPP, S.;GUNDLACH, K., KONSTANTINOVIC, V.S. Effects of radiation therapy on craniofacial and dental implants: a review of the literature. Oral Surgery, Oral Medicine, Oral Pathology, Oral Radiology, and Endodontology, v.107, n.1, p.56–65. 2009.
WANG, L.; YORKE, E.; CHUI, C-S. Monte Carlo evaluation of tissue inhomogeneity effects in the treatmenat os head and neck. Int. J. Radiation Oncology Biol. Phys., v. 50, n. 5, p. 1339–1349. 2001.
WHITE, P. J.; ZWICKER, R. D.; HAUNG, D. T. Comparison of dose homogeneity effects due to electron equilibrium loss in lung for 6 MV and 18 MV photons. Int J Radiat Oncol Biol Phys. v.34, n.5, p.1141-1146. 1996.
ZARZA-MORENO, M; CARREIRA, P.; MADUREIRA, L.; MIRAS DEL RIO, H.; SALGUEIRO, F. J.; LEAL, A.; TEIXEIRA, N.; JESUS, A.P.; MORA, G. Dosimetric effect by shalloe air cavities in high energy electron beams. Physica Medica, v.30, p.234-241. 2014.